A maioria das infecções devido a doenças profissionais são produzidas quando as pessoas manipulam carne ou fluídos corporais potencialmente infectados. Falaremos aqui sobre duas infecções potenciais: erisipelas e S. suis.
Uma doença profissional é qualquer doença que acontece como resultado da prática profissional, pelo que uma pessoa pode estar mais exposta a certas doenças que a população em geral. Uma doença ocupacional pode ser a silicose dos mineiros devido à sua exposição prolongada ao pó das minas ou a perda de audição induzida pelo ruído, nas pessoas que trabalham com maquinaria ruidosa sem protecção auditiva.
Nas cadeias de abastecimento dos porcos, as pessoas que trabalham a diferentes níveis podem estar expostas ao risco de diferentes doenças profissionais devido ao seu trabalho com porcos. Os produtores, médicos veterinários ou transportadores podem ser mordidos por um animal mas, para além do perigo do dano físico, os porcos podem ser portadores de doenças que são potencialmente infecciosas para os humanos e podem ser transmitidas através do contacto ou da manipulação de animais infectados (figura 1). O nível de exposição na exploração ou durante o transporte depende em grande medida do tipo de produção, por exemplo, os produtores comerciais com explorações de centenas ou milhares de animais geralmente não têm um contacto tão próximo com os seus animais e, se o fazem, usam habitualmente equipamentos de protecção. Em países de com baixos salários, onde os porcos são criados principalmente por pequenos agricultores em sistemas de produção extensivos e em contacto com o meio ambiente, as infecções por doenças com origem nos porcos são muito mais comuns e abarcam um amplo espectro que vai desde os parasitas gastrointestinais, brucelose, infecções pelo vírus da gripe suína zoonótica, etc.(Tabela 1).
Tabela 1: Principais zoonoses transmitidas pelos porcos em países em desenvolvimento*
| Principalmente a partir de carne contaminada | Principalmente ocupacionais |
Transmitidas através da ingestão do agente patogénico dentro da carne (p.ex. Trichinella spp.) ou na superfície da carne (p.ex. Cryptosporidium spp. através da água contaminada utilizada para processar a carne)
Ascaris suum Campylobacter spp. Cryptosporidium spp. Echinococcus spp. (toxigénico) Escherichia coli Giardia duodenalis Hepatitis E Listeria spp. Salmonella spp. Sarcystis suihominis Staphylococcus aureus coagulasa-positivo Taenia solium, larval Toxoplasma gondii Trichuris suis Trichinella spp., larval Yersinia enterocolitica |
Transmitidas através do ar (p.ex. Coxiella burnetii), pele (p.ex. Brucella suis) ou vectores (Trypanosoma spp.), especialmente às pessoas expostas com maior frequência a estas rotas de transmissão devido à sua ocupação.
Bacillus anthracis
Brucella suis Coxiella burnetii Erysipelothrix rhusiopathiae Vírus da gripe Leptospira interrogans Complejo Mycobacterium aviumintracelular (MAIC) Raiva Sarcoptes scabiei var. suis Streptococcus suis Trypanosoma spp. Tunga penetrans Ébola (em discussão) |
*Os autores não se responsabilizam pela exaustividade desta lista
No entanto, a maioria das infecções devido a doenças profissionais são produzidas quando as pessoas manipulam carne ou fluídos corporais potencialmente infectados. Falaremos aqui sobre duas infecções potenciais: erisipelas e S. suis.
1. Erisipela suína em humanos
A erisipela suína é causada por uma bactéria chamada Erysipelothrix rhusiopathiae. Muitos mamíferos, peixes e aves em todo o mundo são portadores, mas os porcos são o reservatório mais importante. Também pode sobreviver até um mês na terra. Os porcos podem ser infectados quando a ingerem com terra ou água contaminada e os humanos podem ser infectados quando a bactéria entra na pele humana através de pequenos arranhões ou feridas. É mais provável que isto aconteça durante o abate e posterior processamento das carcaças suínas, quando os trabalhadores manipulam objectos afiados (por exemplo, facas e ganchos) e carne, secreções nasais, urina ou fezes contaminadas sem equipamento de protecção adequado (por exemplo, luvas de aço). Nos porcos, a doença pode causar diferentes lesões, sendo as mais características, na fase aguda, as lesões cutâneas em forma romboidal e de cor vermelha que, frequentemente, são conhecidas como Mal Rubro (figura 2).
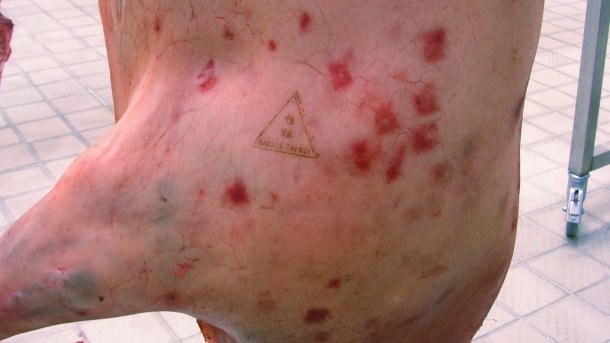
Nos humanos, a infecção pode limitar-se a uma ou duas semanas. No entanto, também pode provocar uma dolorosa infecção cutânea (chamada erisipelóide), frequentemente nas mãos, que pode ser tratada com bastante facilidade com um tratamento antibiótico. Se não for tratada, pode causar febre, dor nas articulações, septicémia e, no pior dos casos, a morte devido a uma infecção cardíaca. A erisipela suína já não é um problema comum na Europa Central porque a vacinação contra as estirpes causadoras da doença nas porcas e nulíparas está disponível e amplamente implementada na maioria das explorações, o equipamento de protecção no matadouro é obrigatório e a população humana está geralmente sã e portanto não tão susceptível. A erisipela, como doença profissional em pessoal que manipula carne crua, parece estar a emergir em países de baixos e médios salários (Musewa et al., na imprensa) onde os sistemas de produção suína são menos rigorosos e há populações humanas de risco, potencialmente imunocomprometidas (p. ex. má nutrição ou presença de doenças que comprometem o sistema imunitário). A bactéria pode ser destruída facilmente com cocção adequada, mas os manipuladores de carne crua de porco, incluindo os que a cozinham, devem tê-lo em conta.
2. Infecção por Streptococcus suis
Os porcos sãos são normalmente portadores da bactéria no nariz e boca, no seu tracto digestivo e urogenital. No entanto, algumas estirpes (em particular o serótipo 2) causam uma doença grave em porcos. Qualquer pessoa que manipule porcos vivos (produtores, médicos veterinários, transportadores, trabalhadores de matadouros) ou carne de porco crua (trabalhadores de matadouros, inspectores de carne, transportadores e cozinheiros) pode estar exposta. A bactéria entra na pele humana através de feridas ou arranhões quase invisíveis e pode replicar-se no sangue (Hughes et al., 2009). Nas pessoas, isto pode provocar septicémia e infecção cerebral que, se não for tratada, pode provocar surdez permanente. Parece haver diferentes estirpes em diferentes áreas geográficas e as estirpes asiáticas são, aparentemente, mais nocivas para os humanos que as estirpes nos países ocidentais. No entanto, nos países industrializados também se podem dar casos de mortalidade. Não foi desenvolvida vacina para porcos nem para humanos, mas pode ser administrado tratamento com antibióticos se a doença for diagnosticada.
Conclusões
Há muitas mais doenças que podem afectar os humanos através do consumo de carne de porco, conhecidas como infecções alimentares e que só causam doenças se ingeridas. Estas incluem, mas não se limitam, a infecções com Campylobacter, Listeria, Salmonella, Yersinia ou Escherichia coli toxigénica, certos complexos de Staphylococcus aureus e Mycobacterium avium intracellulare (MAIC). Quando os consumidores preparam a carne, devem observar regras semelhantes aos dos chefs profissionais nos restaurantes, nunca usar os mesmos instrumentos para cortar alimentos crus e cozidos, ou carne e vegetais, há que proteger a pele de cortes e feridas, evitar tocar a boca e lavar as mãos com água quente no final da preparação dos alimentos.
https://www.3tres3.com.pt/artigos/doencas-profissionais-de-trabalhadores-em-contacto-com-porcos_11441/?utm_source=newsletters333&utm_medium=email&utm_campaign=A+web+em+3+minutos&xemail=aWRtPTcyNzAmaWR1PTUwNzQ0JnQ9NTE1MzY3ZTY2Y2Q4MTFkNjM5MGYzNGQ4ODBmMWVhNGQ%253D






